近期,304am永利集团饶义剑教授团队在建立1,3-二取代四氢异喹啉的化学酶合成新方法方面取得重要进展,研究成果“Modular Chemoenzymatic Cascade for Highly Diastereo- and Enantioselective Synthesis of 1,3-Disubstituted Tetrahydroisoquinolines”正式发表于ACS Catalysis (IF =/info/1021/ /11.7) (https://doi.org/10.1021/acscatal.5c01322)。
1,3-二取代四氢异喹啉(THIQs)广泛存在于天然生物碱中,具有多种生物活性,如β-肾上腺素受体拮抗、抗疟疾和抗HIV活性等。然而,由于该类化合物在THIQ的1,3-位含有特殊的二取代结构,其生物合成途径不明确,关键酶未知,无法通过传统的生物合成方法实现高效生产。为解决上述挑战,本研究设计了一条新的模块化化学酶级联反应途径,克服了生物途径未知的难题,并通过关键酶的半理性改造,实现了一系列1,3-二取代THIQs的高效与高立体选择性合成,并展示了其在制备顺式和反式1,3-二取代THIQs异构体中的潜在应用价值,为生物合成途径不明确的天然产物提供了有效的制备方法,体现了模块化化学酶级联反应在合成生物学领域的广阔前景。
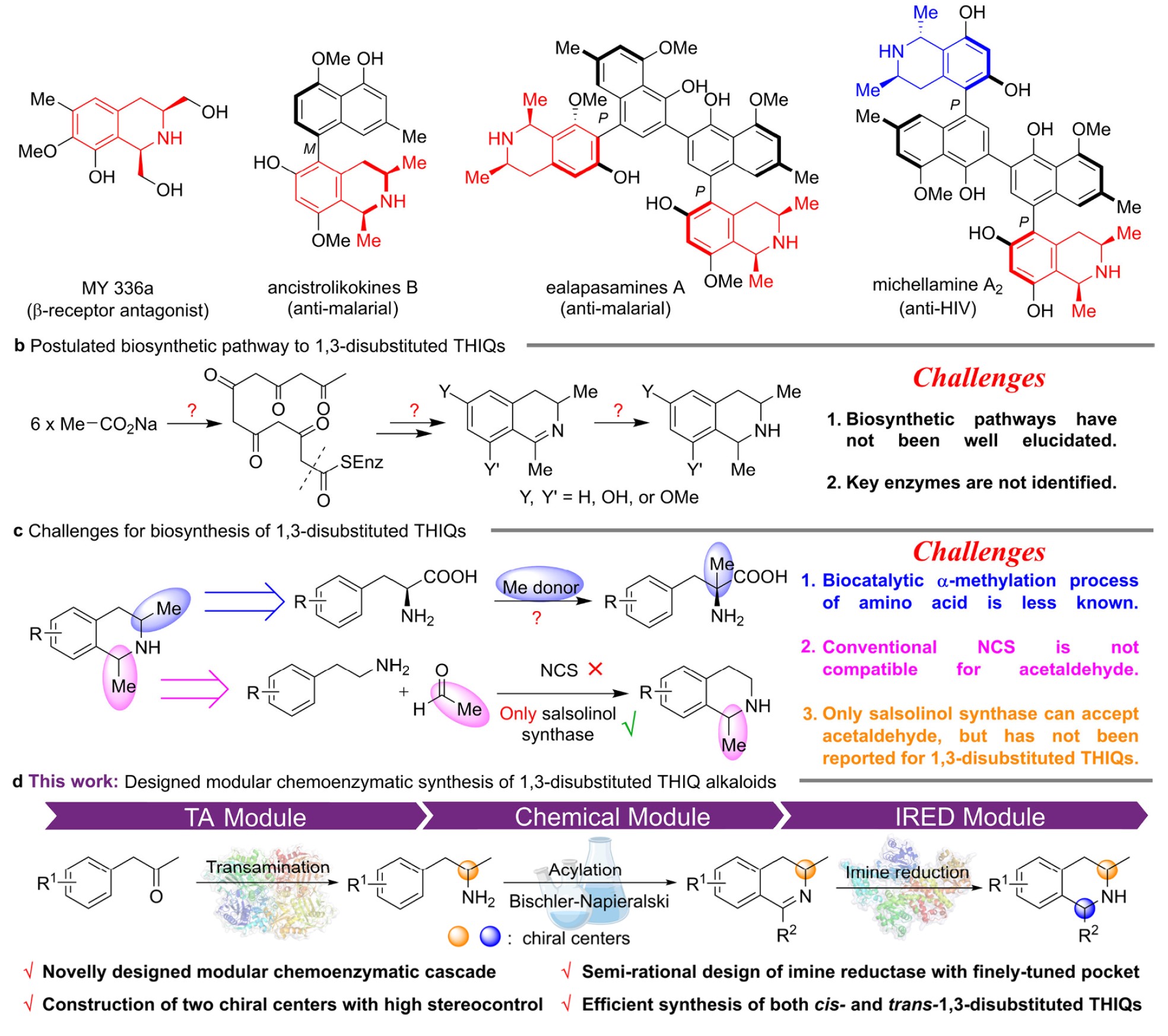
首先,本文基于转氨(TA)、化学和亚胺还原(IRED)三个模块,设计了一种模块化化学酶级联反应,用于从简单易得的非手性底物合成高非对映选择性与对映选择性的1,3-二取代THIQs。通过半理性突变,改造了亚胺还原酶SnIR的活性位点,提高了其催化效率和立体选择性。此外,通过分子动力学模拟和活性位点体积计算,解释了突变体SnIR-MT催化活性、非对映选择性与对映选择性的提升的机制。该级联反应适用于多种底物,能够高效合成多种1,3-二取代THIQs,并展示了其在制备顺式和反式1,3-二取代THIQs异构体中的潜在应用价值。该研究不仅为1,3-二取代THIQs的高效合成提供了一种新方法,还为化学酶级联法合成生物途径未知的复杂天然产物提供了新的思路。
饶义剑教授和袁振波副研究员为论文通讯作者,公司2022级硕士生张洪辉和张艳副教授为共同第一作者。上述工作得到了国家自然科学基金(32270082, 22207044和22477047)、中央高校基本科研业务费(JUSRP124020)、江苏省自然科学基金(BK20202002)的资助。
近年来饶义剑教授团队围绕“天然产物的途径解析与仿生定向合成与应用拓展”开展了系统性的研究,并取得了一系列原创性研究成果,部分成果已发表在Nature Commun (2023,2024,2025),JACS(2024,2025),Angew (2022, 2023,2024),ACS Catal (2020,2021,2022,2024,2025),Green Chem (2019, 2022), Water Res (2022)、 J Hazard Mater (2021, 2023)、 Chem Eng J (2021)等本领域权威期刊。
